Термодинамический цикл - Thermodynamic cycle
| Термодинамика | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|

Классический Тепловой двигатель Карно
|
||||||||||||
|
||||||||||||
|
||||||||||||
А термодинамический цикл состоит из связанной последовательности термодинамические процессы которые включают передача тепла и работай в систему и из нее, при изменении давления, температуры и других переменные состояния внутри системы, и это в конечном итоге возвращает система в исходное состояние.[1] В процессе прохождения цикла рабочая жидкость (система) может преобразовывать тепло от теплого источника в полезную работу, а оставшееся тепло отводить в холодный сток, тем самым действуя как Тепловой двигатель. И наоборот, цикл может быть обращен вспять и использовать работу для перемещения тепла от источника холода и передачи его в теплый приемник, тем самым действуя как Тепловой насос. В каждой точке цикла система находится в термодинамическое равновесие, поэтому цикл обратимый (его изменение энтропии равно нулю, поскольку энтропия является функцией состояния).
Во время замкнутого цикла система возвращается в исходное термодинамическое состояние температуры и давления. Количество процесса (или количества пути), например высокая температура и работай зависят от процесса. Для цикла, для которого система возвращается в исходное состояние, применяется первый закон термодинамики:
Выше указано, что энергия системы не изменяется за цикл. Eв может быть работа и тепловложение во время цикла, а Eвне будет работа и тепловая мощность во время цикла. В первый закон термодинамики также требует, чтобы полезный подвод тепла был равен чистому выходу работы за цикл (мы учитываем тепло, Qв, как положительное и Qвне как отрицательный). Повторяющийся характер технологического процесса позволяет работать в непрерывном режиме, что делает цикл важной концепцией в термодинамика. Термодинамические циклы математически часто представляют как квазистатические процессы при моделировании работы реального устройства.
Тепло и работа
Два основных класса термодинамических циклов: циклы питания и циклы теплового насоса. Циклы мощности - это циклы, которые преобразуют тепловыделение в механическая работа производительность, в то время как циклы теплового насоса передают тепло от низких до высоких температур, используя механическую работу в качестве входа. Циклы, полностью состоящие из квазистатических процессов, могут работать как циклы силового или теплового насоса, контролируя направление процесса. На диаграмма давление – объем (PV) или диаграмма температура – энтропия, то по часовой стрелке и против часовой стрелки направления указывают циклы мощности и теплового насоса, соответственно.
Отношение к работе

Поскольку чистое изменение свойств состояния во время термодинамического цикла равно нулю, оно образует замкнутый контур на Диаграмма PV. Диаграмма PV Y ось показывает давление (п) и Икс ось показывает объем (V). Область, ограниченная петлей, - это работа (W) выполняется процессом:
Эта работа равна балансу тепла (Q), переданного в систему:
Уравнение (2) делает циклический процесс похожим на изотермический процесс: даже несмотря на то, что внутренняя энергия изменяется в ходе циклического процесса, когда циклический процесс завершается, энергия системы равна энергии, которая была у нее в начале процесса.
Если циклический процесс движется по циклу по часовой стрелке, то W будет положительным и представляет собой Тепловой двигатель. Если он движется против часовой стрелки, то W будет отрицательным и представляет собой Тепловой насос.
Каждая точка цикла

Цикл Отто
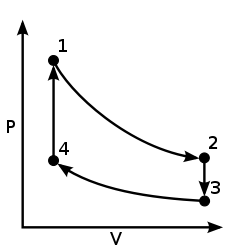
- 1→2: Изэнтропический расширение: постоянное энтропия (s), уменьшение давление (P), увеличение объем (v), уменьшение температура (Т)
- 2→3: Изохорический охлаждение: постоянный объем (v), снижение давления (P), уменьшение энтропии (S), снижение температуры (T)
- 3 → 4: Изэнтропическое сжатие: постоянная энтропия (ы), увеличение давления (P), уменьшение объема (v), увеличение температуры (T)
- 4 → 1: Изохорный нагрев: постоянный объем (v), увеличение давления (P), увеличение энтропии (S), увеличение температуры (T)
Список термодинамических процессов
- Адиабатический : Отсутствие передачи энергии в виде тепла (Q) в течение этой части цикла составило бы δQ = 0. Передача энергии рассматривается только как работа, выполняемая системой.
- Изотермический : В течение этой части цикла процесс находится при постоянной температуре (T = constant, δT = 0). Передача энергии рассматривается как тепло, отводимое от системы или выполняемая ею работа.
- Изобарический : Давление в этой части цикла останется постоянным. (P = константа, δP = 0). Передача энергии рассматривается как тепло, отводимое от системы или выполняемая ею работа.
- Изохорический : Процесс имеет постоянный объем (V = постоянный, δV = 0). Передача энергии рассматривается как тепло, отводимое от системы или выполняемая ею работа.
- Изэнтропический : Процесс имеет постоянную энтропию (S = константа, δS = 0). Передача энергии рассматривается только как тепло, отводимое от системы; система не выполняет никакой физической работы.
- Изентальпический: процесс, который протекает без изменения энтальпии или удельной энтальпии
- Политропный: процесс, подчиняющийся соотношению:
- Обратимый: процесс, в котором производство энтропии равно нулю
Циклы питания

Термодинамические энергетические циклы являются основой работы тепловых двигателей, которые обеспечивают питание большей части мира. электроэнергия и запустить подавляющее большинство автомобили. Циклы питания можно разделить на две категории: реальные циклы и идеальные циклы. Циклы, встречающиеся в реальных устройствах (реальные циклы), трудно анализировать из-за наличия усложняющих эффектов (трения) и отсутствия достаточного времени для установления условий равновесия. Для анализа и проектирования создаются идеализированные модели (идеальные циклы); Эти идеальные модели позволяют инженерам изучать влияние основных параметров, определяющих цикл, без необходимости тратить много времени на проработку сложных деталей, присутствующих в реальной модели цикла.
Энергетические циклы также можно разделить в зависимости от типа теплового двигателя, который они хотят смоделировать. Наиболее распространенные циклы, используемые для моделирования двигатель внутреннего сгорания являются Цикл Отто, какие модели бензиновые двигатели, а Дизельный цикл, какие модели дизельные двигатели. Циклы, которые моделируют двигатели внешнего сгорания включить Цикл Брайтона, какие модели газовые турбины, то Цикл Ренкина, какие модели паровые турбины, то Цикл Стирлинга, какие модели двигатели горячего воздуха, а Цикл Ericsson, который также моделирует двигатели горячего воздуха.

Например, давление-объем механическая работа выход из идеального цикла Стирлинга (чистая выработка), состоящего из 4 термодинамических процессов, составляет[нужна цитата ][сомнительный ]:
Для идеального цикла Стирлинга в процессах 4-1 и 2-3 не происходит изменения объема, поэтому уравнение (3) упрощается до:
Циклы теплового насоса
Циклы термодинамического теплового насоса являются модели для домашнего хозяйства тепловые насосы и холодильники. Между ними нет никакой разницы, за исключением того, что целью холодильника является охлаждение очень небольшого помещения, в то время как бытовой тепловой насос предназначен для обогрева дома. Оба работают, перемещая тепло из холодного помещения в теплое. Самый распространенный цикл охлаждения - это цикл сжатия пара, который моделирует системы с использованием хладагенты эта фаза изменения. В абсорбционный холодильный цикл является альтернативой, которая поглощает хладагент в жидком растворе, а не испаряет его. Циклы охлаждения газа включают в себя обратный цикл Брайтона и Цикл Хэмпсона – Линде. Несколько циклов сжатия и расширения позволяют газовым холодильным установкам сжижать газы.
Моделирование реальных систем

Пример реальной системы, смоделированной идеализированным процессом: диаграммы PV и TS цикла Брайтона, сопоставленные с реальными процессами газотурбинного двигателя
|
Термодинамические циклы могут использоваться для моделирования реальных устройств и систем, обычно путем принятия ряда предположений.[2] упрощающие предположения часто необходимы для сведения проблемы к более управляемой форме.[2] Например, как показано на рисунке, такие устройства газовая турбина или реактивный двигатель можно смоделировать как Цикл Брайтона. Настоящее устройство состоит из серии этапов, каждая из которых моделируется как идеализированный термодинамический процесс. Хотя каждая ступень, которая воздействует на рабочую жидкость, представляет собой сложное реальное устройство, их можно смоделировать как идеализированные процессы, которые приблизительно соответствуют их реальному поведению. Если энергия добавляется другими способами, кроме сжигания, то дополнительное предположение состоит в том, что выхлопные газы будут проходить от выхлопа к теплообменнику, который отводит отработанное тепло в окружающую среду, а рабочий газ будет повторно использоваться на входной ступени.
Разница между идеализированным циклом и реальной производительностью может быть значительной.[2] Например, следующие изображения иллюстрируют различия в результатах работы, прогнозируемые идеальным Цикл Стирлинга и фактическая производительность двигателя Стирлинга:
 |
 |
 |
| Идеальный цикл Стирлинга | Фактическая производительность | Фактическое и идеальное наложение, показывающее разницу в производительности |
Поскольку чистый выход работы для цикла представлен внутренней частью цикла, существует значительная разница между прогнозируемым выходом работы идеального цикла и фактическим выходом работы, показываемым реальным двигателем. Также можно заметить, что реальные индивидуальные процессы расходятся с их идеализированными аналогами; например, изохорное расширение (процесс 1-2) происходит с некоторым фактическим изменением объема.
Хорошо известные термодинамические циклы
На практике простые идеализированные термодинамические циклы обычно состоят из четырех термодинамические процессы. Могут использоваться любые термодинамические процессы. Однако при моделировании идеализированных циклов часто используются процессы, в которых одна переменная состояния поддерживается постоянной, например изотермический процесс (постоянная температура), изобарный процесс (постоянное давление), изохорный процесс (постоянный объем), изоэнтропический процесс (постоянная энтропия) или изэнтальпический процесс (постоянная энтальпия). Часто адиабатические процессы также используются там, где не происходит теплообмена.
Вот некоторые примеры термодинамических циклов и составляющих их процессов:
| Цикл | Сжатие, 1 → 2 | Добавление тепла, 2 → 3 | Расширение, 3 → 4 | Отвод тепла, 4 → 1 | Примечания |
|---|---|---|---|---|---|
| Питание обычно переключается с внешнее сгорание - или циклы теплового насоса: | |||||
| Белл Коулман | адиабатический | изобарический | адиабатический | изобарический | Обратный цикл Брайтона |
| Карно | изэнтропический | изотермический | изэнтропический | изотермический | Тепловой двигатель Карно |
| Ericsson | изотермический | изобарический | изотермический | изобарический | Секунда Цикл Ericsson с 1853 г. |
| Ренкин | адиабатический | изобарический | адиабатический | изобарический | Паровой двигатель |
| Гигроскопичен | адиабатический | изобарический | адиабатический | изобарический | Гигроскопический цикл |
| Скудери | адиабатический | переменное давление и объем |
адиабатический | изохорный | |
| Стирлинг | изотермический | изохорный | изотермический | изохорный | двигатель Стирлинга |
| Мэнсон | изотермический | изохорный | изотермический | изохорный, затем адиабатический | Двигатель Мэнсона-Гиза |
| Стоддард | адиабатический | изобарический | адиабатический | изобарический | |
| Питание обычно переключается с внутреннее сгорание: | |||||
| Брайтон | адиабатический | изобарический | адиабатический | изобарический | Реактивный двигатель. Вариант этого цикла с внешним сгоранием известен как первый Цикл Ericsson с 1833 г. |
| Дизель | адиабатический | изобарический | адиабатический | изохорный | Дизель |
| Ленуар | изохорный | адиабатический | изобарический | Импульсные форсунки. Обратите внимание, что 1 → 2 выполняет как отвод тепла, так и сжатие. | |
| Отто | изэнтропический | изохорный | изэнтропический | изохорный | Бензиновые / бензиновые двигатели |
Идеальный цикл
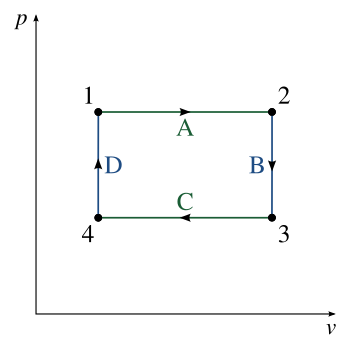
Идеальный цикл состоит из:
- ВЕРХ и ВНИЗ петли: пара параллельных изобарический процессы
- СЛЕВА и ПРАВА от петли: пара параллельных изохорный процессы
Внутренняя энергия идеального газа, совершающего различные части цикла:
Изотермический:
Изохорический:
Изобарический:
Цикл Карно
В Цикл Карно это цикл, состоящий из полностью обратимые процессы из изэнтропический сжатие и расширение и изотермический добавление и отвод тепла. В тепловая эффективность цикла Карно зависит только от абсолютных температур двух резервуаров, в которых происходит теплопередача, а для энергетического цикла составляет:
где это самая низкая температура цикла и самый высокий. Для силовых циклов Карно коэффициент производительности для Тепловой насос является:
и для холодильник коэффициент полезного действия:
Второй закон термодинамики ограничивает КПД и COP для всех циклических устройств до уровней, равных или ниже КПД Карно. В Цикл Стирлинга и Цикл Ericsson два других обратимых цикла, в которых для получения изотермической теплопередачи используется регенерация.
Цикл Стирлинга
Цикл Стирлинга похож на цикл Отто, за исключением того, что адиабаты заменены изотермами. Это также то же самое, что и цикл Эрикссона с изобарическими процессами, заменяющими процессы постоянного объема.
- ВЕРХ и ВНИЗ петли: пара квазипараллельных изотермический процессы
- ЛЕВАЯ и ПРАВАЯ стороны петли: пара параллельных изохорный процессы
Тепло течет в петлю через верхнюю изотерму и левую изохору, и часть этого тепла течет обратно через нижнюю изотерму и правую изохору, но большая часть теплового потока проходит через пару изотерм. Это имеет смысл, поскольку вся работа, выполняемая циклом, выполняется парой изотермических процессов, которые описываются Q = W. Это говорит о том, что все чистое тепло проходит через верхнюю изотерму. Фактически, все тепло, поступающее через левую изохору, выходит через правую изохору: поскольку верхняя изотерма имеет одинаковую более высокую температуру. а нижняя изотерма находится при той же более низкой температуре , и поскольку изменение энергии для изохоры пропорционально изменению температуры, то все тепло, поступающее через левую изохору, компенсируется именно теплом, выходящим из правой изохоры.
Государственные функции и энтропия
Если Z это государственная функция тогда баланс Z остается неизменным в течение циклического процесса:
- .
Энтропия - это функция состояния и определяется как
так что
- ,
тогда оказывается, что для любого циклического процесса
Это означает, что чистое изменение энтропии рабочего тела за цикл равно нулю.
Смотрите также
Рекомендации
дальнейшее чтение
- Холлидей, Резник и Уокер. Основы физики, 5-е изд. John Wiley & Sons, 1997. Глава 21, Энтропия и второй закон термодинамики.
- Ченгель, Юнус А. и Майкл А. Болес. Термодинамика: инженерный подход, 7-е изд. Нью-Йорк: Макгроу-Хилл, 2011. Печать.
- Хилл и Петерсон. «Механика и термодинамика движения», 2-е изд. Прентис Холл, 1991. 760 стр.








































